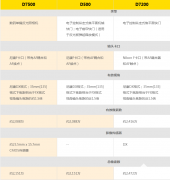
|
ΓΓΓΓΫϋ»’Θ§ΥφΉ≈Ης¥σ“©Τσ¬Ϋ–χ≈ϊ¬Ε2023ΡξQ2≤Τ±®Θ§Ήν–¬ΒΡH1≥©œζ“©TOP10“≤¬Ϋ–χ≥ω¬·ΓΘΥφΉ≈ΡΎΖ÷ΟΎΨόΆΖ≈ΒΚΆ≈ΒΒ¬ΙΪ≤Φ≤Τ±®Θ§Ozempic±μœ÷≥§ –≥Γ‘ΛΤΎΘ§“Μ‘Ψθ“…μΑώΒΞ«ΑΥΡΓΘ ΓΓΓΓ”κ¥ΥΆ§ ±Θ§ΥφΉ≈–¬ΙΎ“©ΈοΚλάϊœϊΆΥΘ§–¬ΙΎ≤ζΤΖΒΡ –≥Γ–η«σ÷π≤ΫΦθ»θΘ§»ΐΩν”…“Ώ«ι―ή…ζΒΡ÷ΊΑθ≤ζΤΖComirnatyΓΔPaxlovidΓΔSpikevaxœζΝΩ÷ηΫΒΘ§Τδ÷–ΒΡ”–ΝΫΩν“―Βχ≥ω«Α °ΘΜ“ΒΡΎ»Υ ΩΤ’±ι»œΈΣΘ§œ¬“Μ≤®άΥ≥±Μρ–μΫΪ”…≥δ¬ζΈόœόεΎœκΒΡΦθΖ “© –≥ûåζΘ§’β“Μ≤¬≤β“―‘Ύάώά¥ΚΆ≈ΒΚΆ≈ΒΒ¬Ωώ≥ΛΒΡΙ…Φέ÷–ΒΟΒΫ”Γ÷ΛΓ≠Γ≠
ΓΓΓΓKeytruda(≈Ν≤©άϊ÷ιΒΞΩΙ) «“Μ÷÷Α–œρ”Ύ≥Χ–ρ–‘œΗΑϊΥάΆω“ρΉ”-1Θ®PD-1Θ©ΒΡ»Υ‘¥Μ·IgG4ΩΙΧεΓΘK“©…œΑκΡξœζ έΕνΦΧ–χ¥¥άζ Ζ–¬ΗΏΘ§¥οΒΫ120.65“ΎΟά‘ΣΘ§Ά§±»‘ω≥Λ20%ΓΘΈΣΝΥ≥…ΨΆK“©Θ§Ρ§…≥ΕΪΫΪ―–ΖΔΆΕ»κ‘ωΦ”ΒΫΑΌ“ΎΟά‘ΣΦΕ±πΘ§Ά§≤ΫΩΣ’Ι ΐ °÷÷ ”Π÷ΔΓΔ…œΑΌœνΝΌ¥≤ ‘―ιΘ§Ά®ΙΐΝΣΚœ”Ο“©ΒΡΖΫΖ®Θ§ΡΟœ¬ΝΥ19Ηω≤ΜΆ§ΒΡ÷ΉΝω ”Π÷ΔΘ§ ΐ °÷÷≤ΜΆ§ΫΉΕΈΒΡ”Ο“©ΖΫΑΗΓΘΗΟ“©ΈοΒΡ≥…ΙΠ”κΡ§…≥ΕΪ«Ω¥σΒΡ―–ΖΔΡήΝΠΚΆ≤ΤΈώΡήΝΠΆ―≤ΜΩΣΙΊœΒΓΘ ΓΓΓΓœ¬ΑκΡξΘ§K“©ΫΪ”≠ά¥–¬Η®÷ζ/Η®÷ζ÷ΈΝΤNSCLCΘ®US/EUΘ©ΓΔ“ΜœΏ“θ–‘ΈΗΑ©Θ®US/EU/JPNΘ©ΓΔHER2―τ–‘ΈΗΑ©Θ®EUΘ©ΓΔΗ®÷ζ÷ΈΝΤNSCLCΒΡ…σ≈ζΨωΕ®“‘ΦΑMerkelœΗΑϊΝωΚΆΕΰœΏ÷ΈΝΤΗΈœΗΑϊΑ© ”Π÷ΔΒΡ»ΪΟφ≈ζΉΦΘΜΜυ”Ύ¥ΥΘ§K“©ΒΡ»ΪΡξœζ έΕν”–Άϊ¥οΒΫ–¬ΗΏΕ»ΓΘ ΓΓΓΓHumiraΘ®–όΟάά÷/ΑΔ¥οΡΨΒΞΩΙΘ©Ήν‘γ”…AbbvieΆΤ≥ωΘ§≤Δ”Ύ2002ΡξΜώΒΟΟάΙζ ≥ΤΖΚΆ“©ΈοΙήάμΨ÷Θ®FDAΘ©≈ζΉΦΓΘΡΩ«ΑΘ§–όΟάά÷»Ϊ«ρΜώ≈ζ ”Π÷Δ“―ΗΏ¥ο17ΗωΘ§Αϋά®άύΖγ ΣΙΊΫΎ―Ή(2002Ρξ)ΓΔ“χ–Φ≤ΓΙΊΫΎ―Ή(2005Ρξ)ΓΔ«Ω÷±–‘ΦΙ÷υ―Ή(2006Ρξ)ΓΔΩΥ¬όΕς≤Γ(2007Ρξ)ΓΔΑΏΩι–Ά“χ–Φ≤Γ(2008Ρξ)ΓΔ«ύ…ΌΡξΧΊΖΔ–‘ΙΊΫΎ―Ή(2008Ρξ)ΓΔάΘ―ώ–‘Ϋα≥Π―Ή(2012Ρξ)ΓΔΜ·≈ß–‘ΝΓΦ≤(2015Ρξ)ΓΔΤœΧ―ΡΛ―Ή(2016Ρξ)Β»ΓΘ ΓΓΓΓ»ΜΕχ‘ΎΟάΙζΘ§HumiraΒΡ –≥ΓΕά’ΦΤΎ“―”Ύ2023Ρξ1‘¬Ϋα χΘΜΫώΡξΡξ≥θΘ§“‘Α≤ΫχΈΣ ΉΩΣΖΔΒΡHumira…ζΈοάύΥΤ“©AmjevitaΫχ»κΟάΙζ –≥ΓΘ§…ζΈοάύΥΤ“©“―Ψ≠ΩΣ Φ≤œ ≥HumiraΒΡœζ έΕνΓΘ≥ΐ¥Υ“‘ΆβΘ§ά¥Ή‘≤ΣΝ÷Ηώ“σΗώΚ≤ΓΔ≈ΒΜΣ…ΫΒ¬ ΩΓΔ≈ΖΦ”¬ΓΓΔΜ‘»πΓΔξΆ÷¬ΓΔCohereusΚΆΖ―…≠”»ΥΙΩ®±»ΒΡHumira…ζΈοάύΥΤ“©“≤ΫΪ”ΎΫώΡξ7‘¬1»’Τπ¬Ϋ–χ‘ΎΟάΙζ…œ –ΓΘ ΓΓΓΓEliquisΘ®ΑΔΏΏ…≥ΑύΘ© «Xa“ρΉ”ΨΚ’υ–‘“÷÷ΤΦΝΘ§”…ΑΌ ±Οά ©Ισ±ΠΘ®BMSΘ©”κΜ‘»πΝΣΚœ―–ΖΔΓΘΑΔΏΏ…≥Αύ”Ύ2011Ρξ5‘¬¬ œ»‘Ύ≈ΖΟΥ≈ζΉΦ…œ –Θ§2012Ρξ12‘¬ΜώΟάΙζFDA≈ζΉΦ…œ –Θ§”Ο”ΎΫΒΒΆΖ«ΑξΡΛ–‘ΖΩ≤ϋΜΦ’Ώ÷–ΖγΚΆ»Ϊ…μ–‘Υ®»ϊΒΡΖγœ’“‘ΦΑ‘ΛΖά…νΨ≤¬ω―ΣΥ®ΒΡ–Έ≥…Θ§2012Ρξ12‘¬Μώ»’±ΨPMDA≈ζΉΦ…œ –Θ§2013Ρξ1‘¬‘Ύ÷–Ιζ≈ζΉΦ…œ –Θ§≤Δ‘Ύ2017ΡξΡ…»κΙζΦ““Ϋ±ΘΡΩ¬ΦΓΘ ΓΓΓΓ”…”ΎΑΔΏΏ…≥Αύ≤ΜΒΪ‘ΛΖάΉδ÷–Θ§Εχ«“ «Ϋω”–ΒΡΕ‘≤Μ “ΥΗχ”ηΜΣΖ®Ν÷÷ΈΝΤΒΡΜΦ’Ώ”κΑΔΥΨΤΞΝ÷Ϋχ––ΓΑΆΖΕ‘ΆΖ±»ΫœΓ±ΒΡΩΙΡΐ“©ΈοΘ§±Μ»œΈΣ «Ζ«ΑξΡΛ–‘ΖΩ≤ϋΜΦ’ΏΫΒΒΆΉδ÷–ΖΔ…ζΦΑ‘ΛΖάœΒΆ≥–‘―ΣΥ®ΒΡάμœκ―Γ‘ώΓΘ¥ΥΆβΘ§ΑΔΏΏ…≥ΑύΡήœ‘Ή≈ΫΒΒΆ―ΣΥ®Η¥ΖΔΚΆ»ΈΚΈ‘≠“ρ‘λ≥…ΒΡΥάΆω»Υ ΐΘ§±Μ”Ο”Ύς≈ΙΊΫΎΜρœΞΙΊΫΎ‘ώΤΎ÷ΟΜΜ θΒΡ≥…ΡξΜΦ’ΏΘ§‘ΛΖάΨ≤¬ω―ΣΥ®Υ®»ϊ ¬ΦΰΘ®VTEΘ©ΓΘ ΓΓΓΓ2017Ρξ8‘¬Θ§ΟάΙζΉ®άϊ…Χ±ξΨ÷ Ύ”ηEliquis“ΜœνΙΊΦϋΉιΚœΈοΉ®άϊΘ§ΫΪΤδ±ΘΜΛΤΎ―”≥Λ÷Ν2026Ρξ11‘¬ΓΘ¥ΥΆβΘ§EliquisΒΡΝμ“Μœν≈δΖΫΉ®άϊ±ΘΜΛΤΎΫΪ”Ύ2031ΡξΒΫΤΎΓΘ‘ΎΉ®άϊ±ΘΜΛΤΎΡΎΘ§Ζ¬÷Τ“©…œ –…––η ±»’Θ§Eliquis –≥ΓΕά’Φ»® «±Θ’œΤδ“ΒΦ®Έ»Ε®‘ω≥ΛΒΡ÷Ί“Σ“ρΥΊΓΘ ΓΓΓΓOzempic «≈ΒΚΆ≈ΒΒ¬ΩΣΖΔΒΡΥΨΟάΗώ¬≥κΡΉΔ…δ“ΚΘ§ΟΩ÷ήΤΛœ¬ΉΔ…δ“Μ¥Έ”Ο”ΎΫΒΒΆ2–ΆΧ«Ρρ≤ΓΜΦ’ΏΒΡ―ΣΧ«Υ°ΤΫΘ§Ά§ ±≈δΚœ“ϊ ≥ΚΆΕΆΝΕΘΜΥϋ“≤”Ο”Ύ“―Ψ≠ΜΦ”––Ρ―ΣΙήΦ≤≤ΓΒΡΧ«Ρρ≤ΓΜΦ’ΏΘ§“‘Αο÷ζΫΒΒΆ÷Ί¥σ–Ρ―ΣΙή ¬ΦΰΒΡΖγœ’Θ§»γ–Ρ‘ύ≤ΓΖΔΉςΜρ÷–ΖγΓΘ≈ΒΚΆ≈ΒΒ¬”ΎΫϋ»’ΙΪ≤ΦΡξ±®Θ§Τλœ¬»ΐΩνΥΨΟάΗώ¬≥κΡ≤ζΤΖOzempicΘ®ΫΒΧ«ΉΔ…δ“ΚΘ©ΓΔRybelsusΘ®ΫΒΧ«Τ§Θ©ΓΔWegovyΘ®Φθ÷ΊΉΔ…δ“ΚΘ©…œΑκΡξΉή ’»κ621.66“ΎΒΛ¬σΩΥά Θ§‘ΦΚœ91.76“ΎΟά‘ΣΘ§ ”Π÷ΔΫΘ÷ΗΫΒΧ«ΚΆΦθ÷ΊΝΫ¥σΝλ”ρΘ§»ΪΡξœζΝΩ”–ΆϊΆΜΤΤ200“ΎΟά‘ΣΘ§”–Άϊ≥…ΈΣœ¬“Μ¥ζΓΑ“©ΆθΓ±ΓΘ ΓΓΓΓBiktarvy «“Μ÷÷»ΐΉιΖ÷÷ΤΦΝΘ§”…»ΥάύΟβ“Ώ»±œί≤ΓΕΨ1–ΆΘ®HIV-1Θ©’ϊΚœΟΗΝ¥ΉΣ“Τ“÷÷ΤΦΝ±»ΩΥΧφά≠ΈΛΘ®50mgΘ©“‘ΦΑΝΫ÷÷HIV-1ΚΥή’άύΥΤΈοΡφΉΣ¬ΦΟΗ“÷÷ΤΦΝΕς«ζΥϊ±θΘ®200mgΘ©ΚΆ±ϊΖ”Χφ≈ΒΗΘΈΛΘ®25mgΘ©Ήι≥…Θ§–Έ≥…ΝΥΩ…”ΟΒΡΜυ”Ύ’ϊΚœΟΗΝ¥ΉΣ“Τ“÷÷ΤΦΝΒΡΉν–Γ3÷÷“©ΈοΒΞΤ§ΦΝΖΫΑΗΓΘ”…”ΎΤδ≤Μ–η“ΣΝΣ”Ο»ΈΚΈΤδΥϊ“©ΈοΘ§Biktarvy‘Ύ…œ –Κσ―ΗΥΌ≥ΤΑ‘HIV –≥ΓΓΘ2022Ρξ11‘¬Θ§ΗΟ“©ΈοΫΪ ”Π÷ΔΆΊ’Ι÷ΝΝΫΥξ«“Χε÷Ί÷Ν…Ό14 kgΒΡHIVΗ–»ΨΕυΆ·Θ§Ϋχ“Μ≤ΫΆΊ’ΙΤδ”Ο“©ΖΕΈßΘ§‘Ύ2023Ρξ≥÷–χ…œΝΩΓΘ ΓΓΓΓDupixent «“Μ÷÷Άξ»Ϊ»Υ‘¥Μ·ΒΡΒΞΩΙΘ§Ω…“÷÷ΤIL-4ΚΆIL-13Ά®¬Ζ–≈Κ≈¥ΪΒΦΘ§≤ύ÷Ί”ΎΨΏ”–2–Ά―Ή÷ΔΒΡΜΦ’Ώ÷ΈΝΤΓΘΉςΈΣ»ϋ≈ΒΖΤœζ έΕνΒΡ÷ς“ΣΙ±œΉ’ΏΘ§Dupixent‘Ύ2023Ρξ…œΑκΡξΉήœζΝΩ54“ΎΟά‘ΣΘ§Ά§±»‘ω≥Λ37%Θ§ ”Π÷ΔΚ≠Η«ΧΊ”Π–‘ΤΛ―ΉΘ®ADΘ©ΓΔœχ¥≠ΓΔ¬ΐ–‘±«-±«ώΦ―ΉΑ鱫œΔ»β (CRSWNP) ΓΔΫαΫΎ–‘―ς’νΓΔ »Υα–‘ ≥Ιή―ΉΓΘ»ΜΕχΘ§Dupixent‘Ύ…œΑκΡξ”≠ά¥ΝΫœνάϊΚΟœϊœΔΘΚ“Μ «ΜώΒΟ≈ΖΟΥ≈ζΉΦ”Ο”Ύ÷ΈΝΤ6Ηω‘¬÷Ν5ΥξΕυΆ·ΒΡ―œ÷ΊΧΊ”Π–‘ΤΛ―ΉΘΜΕΰ «‘Ύ“Μœν’κΕ‘¬ΐ–‘Ήη»ϊ–‘ΖΈ≤Γ(COPD)ΒΡΚσΤΎ ‘―ι÷–»ΓΒΟΝΥ≥…ΙΠΘ§≥…ΈΣΒΎ“ΜΗω“≤ «Έ®“Μ“ΜΗω÷ΛΟς‘Ύ52÷ήΡΎ÷–Ε»Μρ÷ΊΕ»COPDΦ±–‘Φ”÷Ί(ΚτΈϋœΒΆ≥÷ΔΉ¥ΒΡΩλΥΌΚΆΦ±–‘ΕώΜ·)”–ΝΌ¥≤“β“εΚΆΗΏΕ»œ‘Ή≈Φθ…Ό(30%)ΒΡ…ζΈο÷ΤΦΝΘΜ“Σ÷ΣΒάΘ§‘Ύ“‘Μ·“©ΈΣ÷ςΒΦCOPDΝλ”ρ÷–Θ§“―Ψ≠”–10ΕύΡξΟΜ”–»ΈΚΈ–¬ΝΤΖ®Μώ≈ζΓΘΨίΖ÷Έω ΠΆΤ≤βΘ§Χ»»τ¬ΐΉηΖΈ’β“Μ ”Π÷Δ»γΙϊΜώ≈ζΘ§Dupixent…θ÷ΝΩ…Ρή±Θ≥÷43.8%ΒΡΩ÷≤ά‘ω≥Λ¬ ΓΘ ΓΓΓΓStelaraΘ®ΈΎΥΨ≈ΪΒΞΩΙΘ© «“Μ÷÷Ά§ ±Α–œρIL-12ΚΆIL-23ΒΡΒΞΩΥ¬ΓΩΙΧεΘ§”Ύ2009Ρξ Ή¥Έ…œ –Θ§ ”Π÷ΔΑϋά®ΩΥ¬όΕς≤ΓΓΔάΘ―ώ–‘Ϋα≥Π―ΉΚΆΑΏΩιΉ¥“χ–Φ≤ΓΓΘΗΟ“©Έο…œΑκΡξ ’»κ52“ΎΟά‘ΣΘ§Ά§±»‘ω≥Λ7%Θ§”–Άϊ‘ΎΡξΒΉΦΖΫχΑΌ“ΎΟά‘ΣΨψά÷≤ΩΓΘStelara…ζΈοάύΥΤ“©“―¥Π”ΎΦύΙήΙΐ≥ΧΒΡΚσΤΎΫΉΕΈΘ§Amgen”Ύ»ΞΡξ11‘¬ΈΣΤδΚρ―Γ“©ΈοABP 654ΧαΫΜΝΥ“ΜΖίΦρΕΧΒΡ…ζΈο÷ΤΦΝ–μΩ……ξ«κΘ®aBLAΘ©Θ§≤Δ±μ Ψ¥ρΥψ‘Ύ5‘¬ΜώΒΟ‘ΛΤΎ≈ζΉΦΚσΘ§ΫΪΤδ”Ο”ΎStelaraΒΡΥυ”–“―≈ζΉΦ ”Π÷ΔΓΘ«Ω…ζΙΪΥΨ‘ρ‘Ύ»ΞΡξΒΉΧαΤπΥΏΥœΘ§÷ΗΩΊΉ®άϊ‘β ή«÷ΖΗΓΘΫώΡξ5‘¬Θ§«Ω…ζ”κΑ≤Ϋχ¥ο≥…ΚΆΫβΘ§‘ –μΑ≤Ϋχ‘Ύ2025Ρξ1‘¬1»’÷°«ΑΩΣ Φœζ έΤδStelara…ζΈοΖ¬÷Τ“©ΘΜ“ΜΗω‘¬ΚσΘ§«Ω…ζ”κTevaΚΆAlvotech¥ο≥…ΝΥΝμ“Μœν–≠“ιΘ§‘ –μΥϊΟ«‘Ύ2025Ρξ2‘¬21»’÷°«ΑΆΤ≥ωΚρ―Γ“©ΈοAVT04ΘΜΫϋ»’Θ§«Ω…ζΙΪΥΨ–ϊ≤Φ”κFormyconΚΆFresenius Kabi¥ο≥…ΚΆΫβ–≠“ιΘ§’βΝΫΦ“ΙΪΥΨΒΡStelara…ζΈοάύΥΤ“©“≤ΫΪ”Ύ2025Ρξ4‘¬15»’‘ΎΟάΙζΆΤ≥ωΓΘ ΓΓΓΓOpdivoΘ®Ρ…Έδάϊ”»ΒΞΩΙΘ§O“©Θ© «ΒΎ“ΜΗω‘Ύ÷–ΙζΜώ≈ζΒΡPD-1“÷÷ΤΦΝΓΘΫΊ÷ΙΡΩ«ΑΘ§FDA“―≈ζΉΦΗΟ“©Έο11ΗωΑ©÷÷ΒΡ20”ύ÷÷ ”Π÷ΔΘ§ΙζΡΎΜώ≈ζ9Ηω ”Π÷ΔΘ§Κ≠Η«ΖΈΑ©ΓΔΆΖΨ±Α©ΓΔΈΗΑ©ΓΔ ≥ΙήΑ©ΓΔΗΈΑ©ΓΔ…ωΑ©ΓΔΫα÷±≥ΠΑ©ΓΔΡρ¬Ζ…œΤΛΑ©ΓΔΚΎ…ΪΥΊΝωΓΔΜτΤφΫπΝήΑΆΝωΓΔ–ΊΡΛ÷ΉΝωΒ»ΓΘ¥” ”Π÷ΔΜώ≈ζά¥Ω¥Θ§ΗΟ“©ΈοΒΡ ”Π÷ΔΫχ’Ι“Σ‘Ε¬δΚσ”ΎK“©ΓΘ‘ΎΙζΡΎ –≥ΓΩ¥ά¥Θ§ΡΎΨμ―œ÷ΊΒΡPD-1Νλ”ρΘ§Τσ“ΒΖΉΖΉΓΑ≥ωΚΘΓ±―Α«σΚœΉςΘ§≥ΐΝΥΫΒΒΆ…ζ≤ζ≥…±ΨΆβΘ§ΆΊ’Ι ”Π÷Δ≤ΦΨ÷ΓΔΦ”ΥΌ…Χ“ΒΜ· Βœ÷≥…ΙϊΉΣΜ·Θ§Ρ…»κ“Ϋ±Θ’υΕα÷’ΕΥ“Ϋ‘Κ“≤ «ΤδΆΊ’Ι –≥ΓΖίΕνΒΡΙΊΦϋΓΘΡΩ«ΑΘ§ Opdivo “≤‘ΎΜΐΦΪΧΫΥςΟβ“ΏΗ®÷ζ÷ΈΝΤΘ§“‘ΦΑΓΗO+YΓΙΓΔΓΗPD1+LAG3ΓΙΒΡΝΣΚœΝΤΖ®ΓΘ¥ΥΆβΘ§“©ΈοΫΪ”Ύ 2028 Ρξ‘ΎΟάΙζΟφΝΌΉ®άϊΒΫΤΎΘ§ΨίΆΤ≤βΘ§Ϋλ ±…ζΈοΖ¬÷Τ“©ΫΪ«÷ ¥ 56% ΒΡ –≥ΓΓΘ ΓΓΓΓDarzalexΘ®daratumumabΘ© «“ΜΩνΑ–œρΉς”Ο”ΎCD38ΒΡ»Ϊ»Υ‘¥ΒΞΩΥ¬ΓΩΙΧεΘ§ΡήΙΜ“‘ΗΏ«ΉΚΆΝΠΒΡΖΫ ΫΘ§ΧΊ“λ–‘ Ε±π‘ΎΕύΖΔ–‘Ι«ΥηΝωΕώ–‘Ϋ§œΗΑϊ…œΗΏ±μ¥οΒΡCD38Θ§ΫχΕχΆ®ΙΐΕύ÷÷Οβ“ΏΫιΒΦΜζ÷Τά¥”’ΒΦ÷ΉΝωœΗΑϊΒΡΥάΆωΓΘΗΟ“©Έο¥”Ήν≥θΒΡ4œΏ“‘…œ÷ΈΝΤΗ≤Η«ΒΫΡΩ«ΑΒΡ“ΜœΏ÷ΈΝΤΘ§≥…ΈΣΝΥ«Ω…ζΒΡΒΎΕΰΩνΆθ≈ΤΒΞΤΖΓΘΕύΖΔ–‘Ι«ΥηΝωΘ®MMΘ© «Ϋω¥Έ”ΎΖ«ΜτΤφΫπΝήΑΆΝωΒΡΒΎΕΰ≥ΘΦϊ―Σ“Κ÷ΉΝωΘ§Τδ≤ΓάμΧΊ’ςΈΣΙ«Υη÷––ß”ΠBœΗΑϊ“λ≥Θ‘ω÷≥ΖΔ…ζΑ©±δΘ§÷πΫΞΑ―’ΐ≥Θ―ΣœΗΑϊ≈≈≥ΐ‘ΎΆβΘ§¥”ΕχΒΦ÷¬―ΣœΗΑϊΦΤ ΐΫΒΒΆΓΔΙ«÷ ΤΤΜΒΚΆ…ω‘ύΥπ…ΥΓΘ«Ω…ζ‘ΎΙ«ΥηΝωΝλ”ρ≤ζΤΖΦ·ΒΞΩΙΓΔΥΪΩΙΓΔœΗΑϊΝΤΖ®ΈΣ“ΜΧεΘ§≤ΦΨ÷ °Ζ÷Εύ‘ΣΜ·ΓΘΤΨΫηΤδœ»ΖΔ”≈ Τ“‘ΦΑΝΣΚœ÷ΈΝΤΖΫΑΗΒΡ≤ΜΕœΆΊ’ΙΘ§‘ΛΦΤΈ¥ά¥Darzalex»‘ΫΪΦΧ–χ±Θ≥÷Έ»Ε®ΒΡΖΔ’ΙΧ§ ΤΓΘ |